درمان با لوتشیوم دوتاتیت (177Lu-DOTATATE peptide receptor radionuclide therapy; PRRT)
درمان با لوتشیوم دوتاتیت PRRT با آنالوگ های سوماتواستاتین نشاندار (SSAs) به عنوان خط دوم و یا سوم در درمان تومورهای نورواندوکرین (NET) تمایز یافته (گرید 1 و 2) از منشا دستگاه گوارش/پانکراس (GEP-NETs) که علیرغم درمان پیشرفت می کنند، از سال 2018 مورد تایید سازمان غذا و دارو آمریکا FDA قرار گرفته است. در این روش درمان سرطان با پزشکی هسته ای ، SSAs نشاندار شده با ماده رادیواکتیو گیرنده های سوماتواستاتین نوع 2 را در سطح سلول های بدخیم مورد هدف قرار می دهند. اثربخشی درمان تحت تاثیر خواص بیولوژیک PRRT (شامل اتصال به گیرنده و شروع تخریب DNA به علاوه اثر ماده رادیوکتیو) و نیز ویژگی های تومور اولیه (شامل خاستگاه، گرید و میزان بیان گیرنده سوماتواستاتین در سطح سلول بدخیم) قرار دارد.
اثربخشی PRRT
-
کنترل رشد و گسترش تومور
در بیمارانی که تحت درمان همزمان با اکتروتاید و PRRT قرار می گیرند، میزان بقای عاری از پیشرفت (و بر اساس بعضی مطالعات بقای کلی)، به میزان با اهمیتی بالاتر از بیماران تحت درمان با دوز بالای اکتروتاید به تنهایی، گزارش شده است. هرچند در حال حاضر PRRT بهترین انتخاب برای درمان بیماران مبتلا به GEP-NET پیشرفته می باشد، به پاسخ کامل به درمان به ندرت و تنها در کمتر از 3 درصد بیماران رخ می دهد.
-
کنترل علایم
PRRT در کنترل علایم بیماران مبتلا به NET، از جمله سندرم های هورمونی همراه، بسیار موثر است و کیفیت زندگی را در وجوه مختلفی مانند وضعیت کلی سلامت، سطح فعالیت فیزیکی، اسهال، درد و ضعف، حتی بی خواب و کاهش اشتها، در مقایسه با LAR به میزان با اهمیتی بهبود می بخشد. از سوی دیگر، کیفیت زندگی بیماران بدون علامت حین درمان PRRT افتی نشان نمی دهد. بیشترین میزان پاسخ علامتی به PRRT در اسهال، و سپس در درد شکم، گر گرفتگی و ضعف رخ می دهد. به علاوه PRRT درکنترل علایم بیماران مبتلا به سندرم کارسینوئید نیز به عنوان یک روش درمان در نظر گرفته می شود. شواهدی نیز در خصوص بهبود علایم بالینی و اکوکاردیوگرافیک در بیماران مبتلا به کارسینوئید قلبی وجود دارذد. اثرات مثبت مشابهی نیز از درمان با PRRT در کنترل علایم بیماران مبتلا به NET های عملکردی پانکراس شامل انسولینوما، گسترینوما، گلوگاگونوما و VIPoma گزارش شده است.
پیش بینی و پیشگویی پاسخ به PRRT
ساب تایپ های متنوعی از NETs وجود دارد که با پیش آگهی و پاسخ های متفاوت به درمان PRRT همراهی دارند.
- GEP-NETs در مقایسه با non-GEP-NETs بقای عاری از پیشرفت و بقای کلی بالاتری متعاقب درمان PRRT نشان می دهند.
- در گروه GEP-NETs، NETs از منشا پانکراس و روده باریک بقای عاری از پیشرفت بالاتری متعاقب PRRT نسبت به سایر تورمورهای این دسته دارند.
- در مواردی که حجم و وسعت بالای درگیری تومورال وجود دارد، متعاقب PRRT شانس پیشرفت بالاتر و بقای کلی کوتاهتر است.
- در مواردیکه درگیری تومورال بیش از 50 درصد و وجود ضایعات بزرگتر از 3 سانتی متر در کبد وجود دارد. بقای عاری از پیشرفت کوتاهتر است.
- شدت جذب بالای ضایعات در اسکن SSTR قبل از درمان، با پاسخ بهتر متعاقب PRRT همراه است.
- دوز تجمعی رادیوداروی دریافتی، فاکتور مستقل پیش گویی کننده بقا بعد از PRRT می باشد. دوز تجمعی متداول 800 میلی کوری است و در صورتیکه به هر دلیل (مثلا سرکوب مغز استخوان و یا مشکلات کلیوی) ناگزیر به کاهش دوز باشد، بقای پایین تری مورد انتظار است.
- در صورتیکه ضایعات در اسکن 18F FDG PET/CT جذب نشان دهند، بقای کلی پایین تری متعاقب PRRT مورد انتظار است.
- کاهش سطح کروموگرانین سرم متعاقب درمان پیش گویی کننده بقای کلی و بقای عاری از پیشرفت بالاتر می باشد.
پیش بینی و پیشگویی پاسخ به PRRT
پروتکل PRRT
- متداول ترین برنامه درمانی PRRT شامل تجویز 200 میلی کوری 177Lu-DOTATATE به مدت 4 سیکل با فواصل زمانی متوسط 8 هفته (6 تا 10 هفته) می باشد.
- SSAs های طولانی اثر 4 الی 6 هفته و SSA های کوتاه اثر 24 ساعت قبل از هر جلسه درمان لازم است قطع شوند. 2 الی 4 ساعت بعد از پایان درمان شروع مجدد SSAs ها بلامانع است.
- PRRT به صورت سرپایی قابل انجام است.
- متوسط 1 هفته قبل از هر جلسه درمان و 2 الی 3 هفته متعاقب هر جلسه درمان، بررسی سطح سلول های خونی و نیز عملکرد کبد و کلیه ضروری است.
- ارزیابی پاسخ به درمان توسط روش های تصویر برداری، 2-3 ماه و 6 ماه بعد از اتمام کورس درمان PRRT انجام می شود.
Salvage PRRT
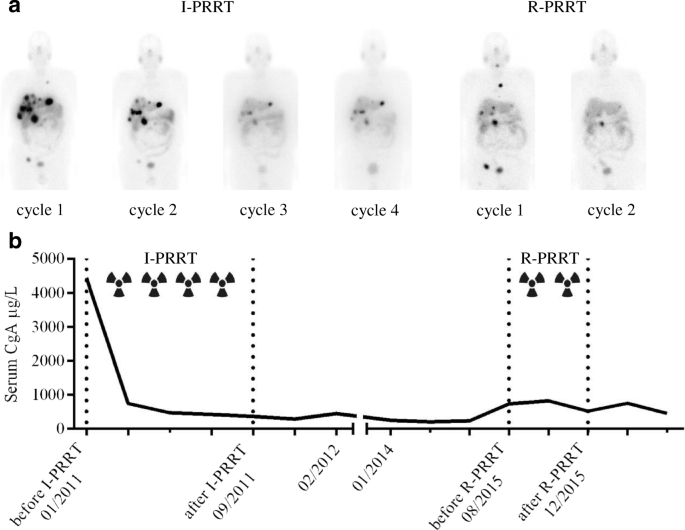
در بیمارانی که PRRT با پاسخ اولیه مناسب به درمان همراه است، در صورت بروز پیشرفت بیماری، در فاصله حداقل 18 ماه، می توان یک درمان اضافی با 2 سیکل لوتشیوم دوتاتیت با دوز 200 میلی کوری برای بیمار در نظر گرفت. هر چند میزان پاسخ به درمان و بقا در salvage PRRT در مقایسه با کورس درمانی اولیه پایین تر است، معهذا می تواند در مواردی که سایر درمان های سیستمیک با شکست مواجه شده اند، یک انتخاب درمانی باشد. در صورت پاسخ مناسب به salvage PRRT می توان در موارد بعدی پیشرفت بیماری نیز re-treatment با PRRT یا R-PRRT را مد نظر قرار داد.
ملاحظات کلی در انتخاب بیمار
از آنجاییکه کارآزمایی های بالینی بر روی مقایسه مستقیم انواع روش های درمانی در حال حاضر وجود ندارد، انتخاب و توالی روش های درمانی مبتنی بر شواهد نیست و تصمیم گیری می باید بر اساس مقایسه نتایج کارآزمایی های بالینی و سنجش مضار و منفعت هریک از روش های درمانی در هر بیمار به صورت جداگانه انجام شود.
انتخاب بیمار
PRRT در درمان بیماران مبتلا به GEP-NETs که علیرغم درمان با SSA شواهد پیشرفت بیماری (اعم از علامتی یا رادیولوژیک) را نشان می دهند، توصیه می شود. به دلیل اثر بخشی و ایمنی دراز مدت SSA، استفاده از PRRT به عنوان خط اول درمان توصیه نمی شود. از جمله موارد استثنا بیمارانی هستند که بالک خیلی وسیع تومورال دارند و هرگونه افزایش بیشتر در رشد تومور بالقوه ممکن است تهدید کننده باشد.
-
Midgut
در NETs های تیپیک مترشحه هورمون از منشا میدگات، درمان های سیستمیک متعاقب خط اول درمان SSA، محدود هستند و اضافه کردن everolimus به درمان اکتروتاید با بهبود چشمگیر در بقای عاری از پیشرفت همراه نبوده است. به همین دلیل، PRRT به عنوان choice خط دوم درمان در این بیماران محسوب می شوند. در خصوص انتخاب PRRT یا everolimus به عنوان خط دوم درمان در NETsهای فاقد عملکرد از منشا GI، تصمیم گیری به صورت فرد-محور و با در نظر عوامل دیگر از جمله میزان بیان گیرنده های سوماتواستاتین بر مبنای یافته های اسکن SSTR قبل از درمان می باشد.
-
پانکراس
برای panNETs درمان های سیستمیک متعدد از جمله درمان های هدفمند (everolimus وsunitinib) و شیمی درمانی (capecitabin/temozolamide) وجود دارند. شواهدی مبنی بر اثر بخشی بهتر PRRT در مقایسه با sunitinib وجود دارد و در مورد everolimus مطالعات در حال انجام است. هرچند شیمی درمانی در انواع تومورهای تهاجمی تر و علامتدار، احتمالا انتخاب بهتری است و در سایر موارد، اثربخشی تقریبا یکسان میان شیمی درمانی و PRRT گزارش شده است، همچنان مطالعات بیشتری مورد نیاز است تا بتوان در مورد توالی انتخاب این روش های درمانی نسبت به یکدیگر اظهار نظر کرد.
-
Bronchial/Pulmonary
در بیمارانی که علیرغم درمان با everolimus شواهد پیشرفت نشان می دهند، می توان به شرط مثبت بودن یافته های اسکن SSA قبل از درمان، به ویژه در تومورکارسینوئید تیپیک و احتمالا آتیپیک، PRRT را مد نظر قرار داد. در این گروه از بیماران شروع PRRT قبل از everolimus توصیه نمی شود.
تومورهای نورواندوکرین از منشا نامشخص
هرچند مطالعه ای که منحصرا بر روی این گروه از بیماران انجام شده باشد، وجود ندارد، به نظر می رسد که اثر بخشی PRRT در این بیماران، مشابه NETs دارای منشا شناخته شده از دستگاه گوارش و پانکراس می باشد. بنابراین همانند بیماران مبتلا به GEP-NETs، در بیماران مبتلا به تومورهای نورواندوکرین از منشا نامشخص که علیرغم درمان خط اول با آنالوگ های سوماتواستاتین شواهد پیشرفت بیماری را نشان می دهند، می توان درمان با لوتشیوم دوتاتیت را در نظر گرفت.
-
پاراگانگلیوما/فئوکروموسیتوما
131I MIBG درمان مورد تایید FDA در بیماران مبتلا به پارا/فئو می باشد. هرچند نتایج مطالعات در خصوص اثر بخشی PRRT با لوتشیوم دوتاتیت در این بیماران، امیدوار کننده است، در حال حاضر PRRT تنها در آن دسته از بیماران فئو/پارا که جذب MIBG نشان نمی دهند، توصیه می شود.
-
نورواندوکرین کارسینوماها و تومورهای نورواندکرین گرید 3
در این گروه از تومورها، PRRT درمان استاندارد محسوب نمی شود. PRRT ممکن است در تورموهای دارای Ki-67 زیر 55 درصد، به شرط آنکه تمام ضایعات در اسکن SSAs قبل از درمان جذب نشان دهند، در نظر گرفته شود.
بیمارن واجد شرط PRRT با لوتشیوم دوتاتیت
بیمارن واجد شرط PRRT با لوتشیوم دوتاتیت
- وجود جذب مناسب در تمام ضایعات در اسکن SSAs قبل از درمان.
- منظور از جذب مناسب، جذبی برابر با کبد در اسکن 99m Tc-Octreotide Scintigraphy و بیش از کبد در اسکن 68Ga-DOTATATE PET/CT می باشد.
- سطح فعالیت فیزیکی مناسب
- عدم ابتلا به بیماری قلبی شدید
- عدم بارداری و شیردهی
- Life expectancy بیش از 3 ماه
- پروفایل مناسب آزمایشگاهی شامل CBC، کبد و کلیه
گردآوری شده توسط مرکز پزشکی هسته ای اکسیر هلف








